作为一名长期关注神经科学发展的自媒体创作者,我最近被一个前沿话题深深吸引——那就是光遗传技术、小胶质细胞、启动子和血清型这几个关键词的结合。
这些看似专业术语的词汇,其实正在悄悄改变我们对神经系统疾病的理解和治疗方式。今天,我想用通俗易懂的语言,带你一起走进这个充满希望的研究领域。
光遗传技术的崛起
还记得几年前第一次听到“光遗传”这个词的时候,我以为是科幻小说里的设定。但如今,这项技术已经广泛应用于神经科学研究中,甚至在某些实验中展现出惊人的潜力。
简单来说,光遗传技术就是利用光来控制特定的神经元活动。科学家通过基因工程技术,在目标细胞中表达光敏感蛋白,这样就可以用不同波长的光来激活或抑制这些细胞的功能。
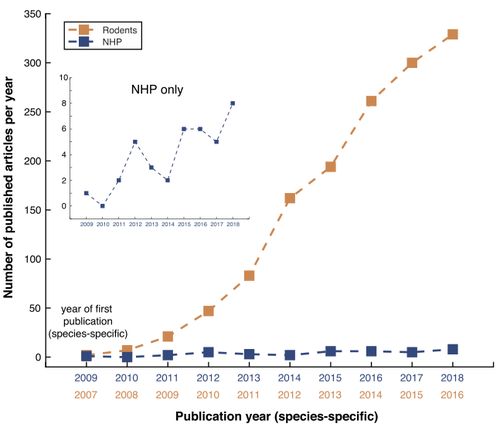
比如在一项针对Nf1OPG小鼠的研究中,科学家使用光遗传学技术刺激小鼠视网膜和视神经的外植体,结果发现神经元活动增加后,两种关键蛋白的分泌确实提升了。这说明神经元活动可以调控蛋白分泌,而这可能为某些神经系统疾病提供新的治疗思路。
小胶质细胞的角色转变
过去,小胶质细胞一直被认为是大脑中的“清洁工”,主要负责清除死亡细胞和碎片。但近年来的研究表明,它们的作用远不止于此。
特别是在脑创伤后,小胶质细胞会被诱导进入三种不同的激活状态:iMG-1(促炎型)、iMG-2(调控型)和iMG-3(吞噬型)。其中,iMG-1在所有年龄段都会出现,而iMG-2和iMG-3则分别从幼年晚期和成年阶段开始出现。
这意味着,小胶质细胞不仅参与炎症反应,还可能在神经修复和免疫调节中发挥重要作用。
更令人惊讶的是,研究人员首次实现在非老龄化小鼠中引入了老龄化的小胶质细胞。他们发现,仅仅让小胶质细胞老化,就能引起小鼠认知功能的衰退。这为我们理解衰老相关神经退行性疾病提供了全新的视角。
启动子与血清型的协同作用
在基因治疗中,启动子和血清型的选择至关重要。启动子决定了基因在哪些细胞中表达,而血清型则影响着病毒载体的感染效率和靶向性。
例如,在使用AAV(腺相关病毒)进行基因递送时,选择合适的血清型可以显著提高目标细胞的转染效率。同时,启动子的特异性也决定了基因表达的空间分布和强度。
这种精准调控的能力,使得科学家可以在特定类型的神经细胞中启动或关闭某些基因,从而研究其功能。这也为未来的个性化治疗奠定了基础。
ZNF638与胶质母细胞瘤的秘密
说到胶质母细胞瘤(GBM),这是目前最致命的一种脑肿瘤之一。最近有研究发现,ZNF638在胶质母细胞瘤组织中的表达水平显著高于正常脑组织,这提示它可能在肿瘤发生发展中扮演重要角色。
为了验证这一点,研究人员对大量患者样本进行了基因表达分析,并进一步利用shRNA技术敲低PHGDH(一种与代谢相关的酶)。结果显示,Aβ聚集减少,突触损失和细胞凋亡也随之减轻。
这一发现不仅揭示了ZNF638和PHGDH在神经退行性疾病中的潜在机制,也为未来的靶向治疗提供了新思路。
NMDAR-Ptgs2通路与脑损伤治疗
创伤性脑损伤(TBI)是一个全球性的健康问题。最新的研究表明,TBI可以显著激活神经元上的NMDAR-Ptgs2通路,并引发包括星状胶质细胞和小胶质细胞在内的胶质细胞激活和增殖。
当NMDAR被抑制时,这种激活效应也随之减弱。这说明NMDAR可能是治疗TBI的一个关键靶点。
此外,研究还发现,不同年龄的小鼠在脑创伤后的反应也有所不同。少突胶质细胞的成熟和髓鞘化始于幼年晚期并持续至成年阶段,分化出三种成熟亚型(MOL1/2/3)。这提示我们在开发治疗方法时,必须考虑患者的年龄因素。
结语:未来已来
科技的发展总是超出我们的想象。从光遗传到小胶质细胞调控,从启动子设计到血清型优化,每一个突破都在推动我们离治愈神经系统疾病的目标更近一步。
作为一名普通读者,也许你并不需要理解每一个分子机制,但你可以感受到——我们正站在一个医学革命的门槛上。

发表评论 取消回复