导读:引言 | EGFR靶向治疗现状 | 帕尼单抗的突破性进展 | 耐药机制解析 | 未来展望与患者希望
引言:从“精准”到“更精准”的抗癌之路
作为一名长期关注肿瘤治疗领域的自媒体写作者,我一直在追踪那些能真正改变癌症患者命运的新技术、新药物。最近,关于EGFR靶向治疗在结直肠癌中的最新研究引起了我的极大兴趣。
尤其是帕尼单抗(Panitumumab)作为新一代EGFR抑制剂,在解决传统EGFR抗体药物如西妥昔单抗(Cetuximab)所面临的耐药问题上,展现出令人振奋的潜力。
EGFR靶向治疗现状:为何它曾是结直肠癌患者的曙光?
早在2010年代初,EGFR靶向治疗就为RAS/BRAF野生型转移性结直肠癌(mCRC)患者带来了前所未有的生存延长机会。像西妥昔单抗和帕尼单抗这类药物,通过阻断表皮生长因子受体(EGFR)信号通路,有效抑制了癌细胞的增殖。
“对于基因检测显示RAS/BRAF未突变的患者来说,EGFR靶向治疗几乎是‘量身定制’的救命稻草。”——某三甲医院肿瘤科主任
然而,好景不长,很多患者在接受治疗一段时间后,逐渐出现了耐药现象,导致疗效大打折扣。
帕尼单抗:为何被称为“EGFR治疗的升级版”?
相比西妥昔单抗,帕尼单抗是一种全人源化的IgG1单克隆抗体,理论上具有更强的亲和力和更低的免疫原性。临床试验数据显示,帕尼单抗在一线治疗中显示出更优的无进展生存期(PFS)。
尤其是在KRAS/NRAS/BRAF野生型患者群体中,帕尼单抗联合化疗方案显著提高了客观缓解率(ORR),并延长了总生存期(OS)。
但即便如此,耐药问题依然存在,甚至部分患者在初始治疗阶段就表现出原发性耐药。
耐药机制揭秘:肿瘤异质性与旁路激活
近年来的研究表明,EGFR靶向治疗失败的主要原因包括:
- 肿瘤细胞内部的KRAS/NRAS突变激活
- EGFR胞外域突变(如S492R)导致抗体结合障碍
- 其他信号通路的代偿性激活(如MET扩增、HER2过表达)
- 肿瘤微环境中免疫逃逸机制增强
以北京大学肿瘤医院的一项研究为例,他们发现某些患者在接受EGFR靶向治疗后,体内出现了MET通路异常激活的现象,这直接导致了对EGFR抑制剂的耐药。
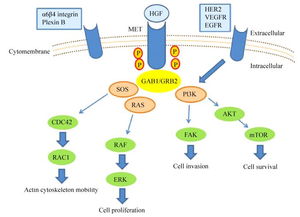
未来展望:如何打破耐药魔咒?
面对耐药这一难题,科学家们正在尝试多种策略来“破局”,其中包括:
- 开发新一代EGFR抑制剂,如双特异性抗体(如Amivantamab)
- 联合使用多靶点药物,如EGFR + MET双重抑制
- 引入免疫检查点抑制剂,如PD-1/PD-L1抗体
- 个性化治疗:基于循环肿瘤DNA(ctDNA)动态监测调整治疗方案
例如,有研究团队正在探索将帕尼单抗与BMS-813160(CCR2/5抑制剂)及纳武利尤单抗联合使用的方案,初步结果显示该组合在边缘可切除或局部晚期胰腺癌中具有一定疗效。
此外,随着NGS(下一代测序)技术的普及,越来越多的患者能够在治疗初期就明确自身的基因突变状态,从而实现真正的个体化用药。
结语:希望就在前方
虽然EGFR靶向治疗在结直肠癌中面临挑战,但帕尼单抗的出现无疑为我们打开了一扇新的窗户。随着对耐药机制的深入理解以及新型药物的研发推进,我们有理由相信,未来的结直肠癌治疗将更加精准、高效。
作为一名长期关注肿瘤医学的写作者,我将持续追踪这些前沿进展,并第一时间与大家分享。




发表评论 取消回复